LA STIBINE ET SA LIQUATION
StibineQuelques autres noms suivant la tradition : Stibium – Alcofol – Othia – Alkosol – Bélier – Saturne des philosophes – Fils et gendre de Saturne – Lion rouge – Loup – Racine des métaux – Prothée – Plomb sacré – Plomb des sages ou des philosophes – Antimoine de la mine – etc. |
 |
 |
 |
 |
|
Ce trisulfure était autrefois très abondant en France. Nous avions, après deux années de tractations avec le BRGM et l’exploitant, obtenu d’acheter, en le sélectionnant nous-mêmes,[photo 5] du minerai brut, (dont nous avons obtenu un rendement moyen de 51,6 %) au moment précis de l’ouverture d’une mine en Bretagne. Nous avions également pour la suite une option pour obtenir du minerai purifié, une fois que l’installation de concentration par flottaison (en construction) serait achevée.
Malheureusement cette installation ne fut même pas terminée et la mine, pourtant très riche fut fermée et rebouchée, ceci uniquement pour des raisons de prix de revient par rapport au minerai d’importation. Il ne faut tout de même pas désespérer, nous avons le souvenir de fructueuses récoltes, notamment dans le lit du ruisseau de la mine de la Bessade, [photo 6] (dont nous avons obtenu un rendement moyen de 25,9 %). Pour ce qui est du minerai français, il semble que la Corse présente encore des possibilités, mais c’est l’importation qui devient de plus en plus la source incontournable. Les très petites quantités que l’on peut encore trouver en fouillant les anciennes galeries dangereuses [photo dissuasive 7] et les haldes des mines abandonnées sont de trop faible rendement [voir annexe]. Ce type de recherche est de plus formellement interdit par la loi qui protège les mines en tant que patrimoine archéologique industriel. En effet, au-dessous d’un certain pourcentage de stibine dans le minerai, la gangue la retient par capillarité lors de l’incontournable opération de « liquation » (séparation d’avec la gangue). Notre propre installation de flottaison (utilisée à contre cœur, à une époque où nous devions impérativement concentrer du minerai pauvre), consistait à faire arriver un petit courant d’air (gonfleur sur perceuse), dans le fond d’une grosse machine à laver cylindrique[photo 8], dans laquelle le minerai broyé (pulpe) barbotait (machine avec agitateur circulaire plat, en fond de cuve) dans de l’eau additionnée de très très peu de liquide vaisselle (à défaut d’un des produits chimiques spéciaux introuvables, par exemple l’éthylxanthate de potassium ; on aurait dû également y adjoindre de l’essence de pin). Le principe de ce dispositif repose sur la propriété qu’ont les bulles ainsi formées de se fixer sélectivement aux grains de stibine (ou d’un autre minerai, souvent un sulfure), qui ont la propriété de ne pas être mouillés si le pH est convenable, et si le calibrage du minerai est correct, grains de 0,2 à 0,05 mm et de les porter en surface. Pour simplifier l’installation, nous les recueillions simplement à l’écumoire. Il n’en reste pas moins que ce travail est long et peu gratifiant bien que le rendement final en poudre de stibine récupérée soit proche de 90%. |
 |
 |
 |
 |
|
Si vous disposez d’un peu de minerai riche, vous pouvez en le plaçant au dessus du minerai pauvre, mouiller ce dernier par le flux de stibine qui s’écoule du dessus, et ainsi en récupérer une partie (si par contre il n’y a pas assez de minerai riche vous perdrez presque tout !). Cette pratique fut industriellement utilisée par l’adjonction dite d’un « troisième pot » sur l’ensemble des deux premiers : pot à stibine et pot à minerai, constituant « l’ensemble à régule », commercialisé, mais mal nommé car il n’y a pas de régule à ce stade.
Pour mémoire (nous ne pouvons en parler car nous n’avons encore que peu d’expérience), certain effectuent actuellement un grillage à l’air des minerais pauvres broyés, et après condensation sur une grande surface froide, des vapeurs blanches qui se dégagent, recueillent de la poudre de trioxyde d’antimoine, puis réduisent l’oxyde obtenu. Nos réductions sous poudre de charbon de bois tassé sont sans problème mais l’opération est non canoniques car excluant la » tête morte » du premier régule et le » ferment » récupéré lors de la liquation. Autre méthode ancienne, (industrielle et non canonique), griller le minerai (en restant au-dessous de la chaleur rouge sombre qui amorce la fusion du sulfure présent). Comme il faut remuer la matière régulièrement pendant 12 heures, pensez à respirer autre chose ! Industriellement, cette méthode « grillage volatilisant » fut employée en grillant le minerai, (constamment remué) étalé sur de larges soles, et en aspirant les vapeurs d’oxysulfure Sb2O3, (désignées dans le commerce par le nom « d’oxyde soluble ») puis en les faisant passer (avant le ventilateur) dans un brouillard d’eau pulvérisée. Le mélange eau et oxyde était récupéré dans des bassins où l’oxyde se déposait. L’oxyde servait dans la fabrication de peintures ou était réduit en régule. Liquation : |
 |
 |
 |
 |
 |
 |
 |
|
On dispose sous le four un réceptacle plein d’eau (grand bocal en verre ou grès, d’au moins 20 cm. de haut car la stibine très chaude colle à une cuvette plastique et fend le verre si elle est encore trop chaude lors du contact). Il est destiné à recueillir les gouttes de stibine en fusion qui s’écoulent du four [photo 16 ], parfois en cataracte dont le flux mal dirigé génère des stalactites[photo 17].
Cette stibine dépose une « mousse » de couleur rougeâtre à la surface de l’eau [photo 18]. On la récupère (précieusement pour la suite) ainsi que celle qui s’est mêlée à l’eau du vase, en rinçant soigneusement la stibine, [photos 19, 20, 21, 22]. Une fois déposée et séchée, il ne reste de cette mousse qu’une très faible quantité de poudre rouge, [photos 23 & 24]. |
 |
 |
 |
 |
 |
 |
 |
 |
 |
|
Mise en garde :
Se garder de respirer les fumées riches en arsenic qui se dégagent, et porter des gants car l’arsenic passe aussi dans les petites coupures ou irritations de la peau. ANNEXE : |
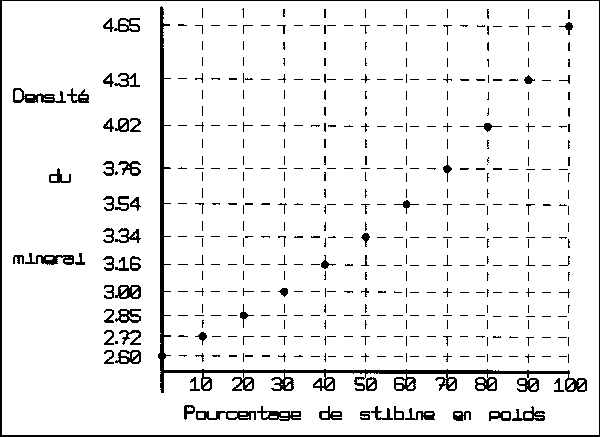 |
Les Amis de l’Alchimie. |
